混合型高脂血症は、低密度リポタンパク質 (LDL) とトリグリセリドに富むリポタンパク質の血漿レベルの上昇を特徴とし、この患者集団ではアテローム性動脈硬化性心血管疾患のリスク増加につながります。
ANGPTL3は、リポタンパク質リパーゼおよびエンドセプターゼを阻害し、さらにトリグリセリドを多く含むリポタンパク質の肝臓への取り込みを阻害します。ANGPTL3不活性化変異体の保有者は、トリグリセリド、LDLコレステロール、高密度リポタンパク質(HDL)コレステロール、非HDLコレステロールの値が低く、動脈硬化性心血管疾患のリスクも低下していました。ゾダシランは、肝臓におけるANGPTL3の発現を標的とする低分子干渉RNA(RNAi)薬です。
混合型高脂血症とは、低密度リポタンパク質コレステロール(LDL-C)とトリグリセリドを多く含むリポタンパク質の値が上昇した状態を指します。トリグリセリドを多く含むリポタンパク質(カイロミクロン、超低密度リポタンパク質(VLDL)、残留コレステロールを含む)は、動脈硬化性疾患の発症に重要な役割を果たします。混合型高脂血症には効果的な治療法はありません。
ベイツ系薬剤はトリグリセリド(TG)値を低下させることが知られていますが、その低下効果は限定的です。同時に、ベイツ系薬剤を含むTG低下薬(エイコサペンタエン酢酸など)は、残留コレステロール値の上昇に起因する動脈硬化性疾患のリスクに有意な効果を示していません。さらに、スタチンを既に服用している患者を対象とした過去の研究では、TG低下薬の併用は心血管イベントのリスクを低下させないことが示されています。これらの要因により、混合型高脂血症の治療は非常に困難になっています。
ANGPTL3(アンジオポエチン様タンパク質3)は、リポタンパク質リパーゼ、エンドセプターゼ、および低密度リポタンパク質(LDL)受容体依存性肝リポタンパク質の取り込みを可逆的に阻害することにより、TGおよび非高密度リポタンパク質コレステロール(HDL-C)を含む脂質およびリポタンパク質代謝を制御します。ANGPTL3の不活性化変異体は、リポタンパク質リパーゼおよびエンドセプターゼの活性を上昇させ、その結果、ほとんどの場合、血漿リポタンパク質濃度が低下することが分かっています。これには、トリグリセリドに富むリポタンパク質(すなわち、カイロミクロン、残留コレステロール、VLDL、中密度リポタンパク質[IDL])、LDL、高密度リポタンパク質(HDL)、リポタンパク質(a)、およびそれらのコレステロール成分が含まれます。この変異を有するヘテロ接合性患者は、動脈硬化性疾患のリスクが約40%低下し、有害な臨床的表現型は認められていません。ANGPTL3は肝臓で発現しており、そのmRNAを標的とした遺伝子サイレンシング療法(低分子干渉RNA(siRNA)薬)は、高脂血症の有望なハイブリッド治療法です。
2024年9月12日、ニューイングランド・ジャーナル・オブ・メディシン(NEJM)誌に、siRNA薬ゾダシランが混合型高脂血症患者のTG値を有意に低下させたことを確認するARCHES 2試験が掲載されました[1]。ARCHES-2は、二重盲検プラセボ対照用量範囲探索第2b相試験です。混合型高脂血症(空腹時TG値150~499 mg/dL、LDL-C値70 mg/dL以上、またはnon-HDL-C値100 mg/dL以上)の患者204名が登録されました。患者はゾダシラン50 mg群、100 mg群、200 mg群、プラセボ対照群に分けられました。患者は1週目と12週目に皮下注射を受け、36週目まで追跡予防を受けました。
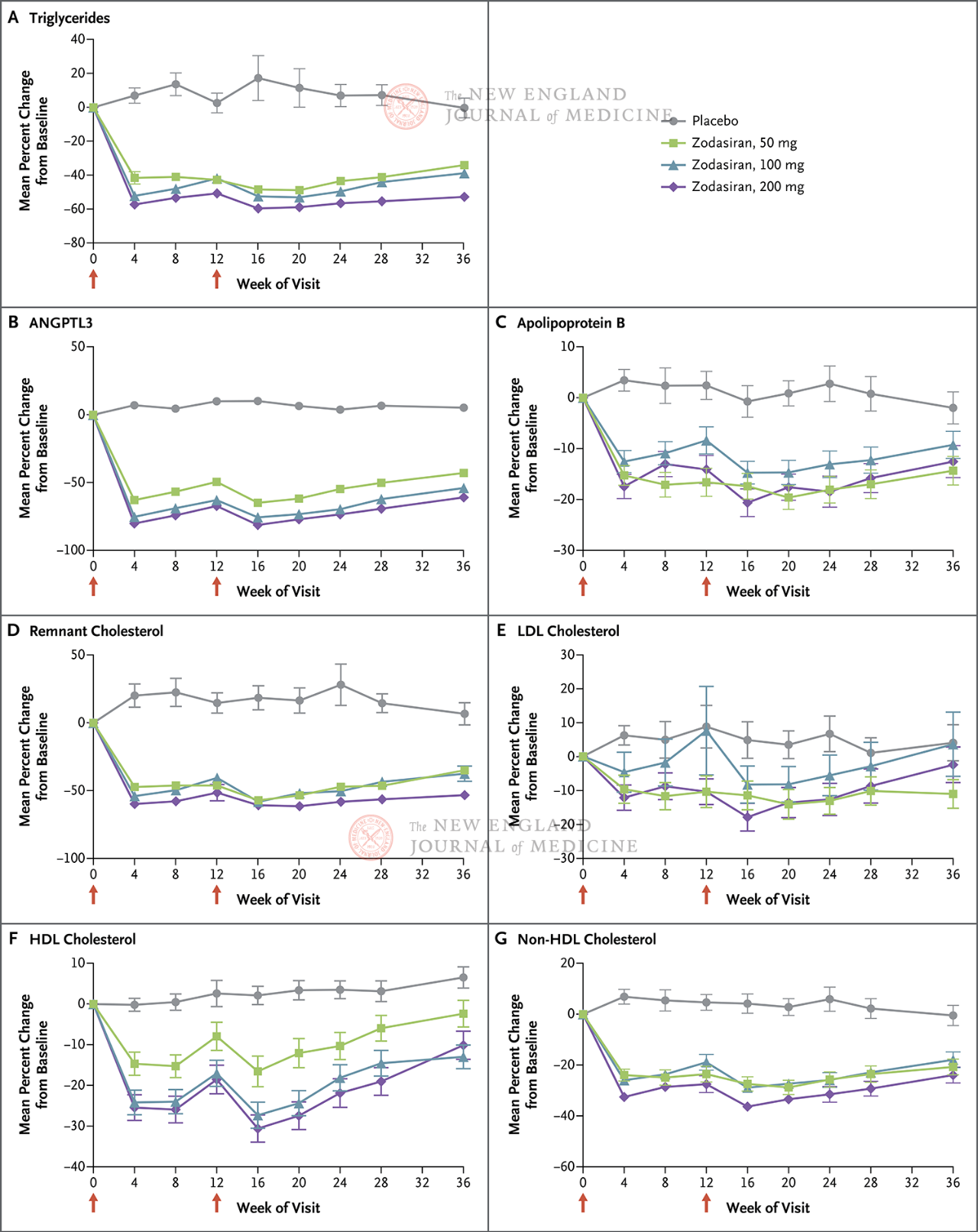
主要評価項目は、ベースラインから24週までのTGの変化率であった。試験では、24週までにゾダシラン群のTGレベルが用量依存的に有意に減少した(プラセボ群と比較して、各用量群のTGレベルはそれぞれ51、57、63パーセントポイント減少した)(すべての比較でP<0.001)。ANGPTL3もそれぞれ54パーセントポイント、70パーセントポイント、74パーセントポイント減少した。非HDLコレステロール値はそれぞれ29パーセントポイント、29パーセントポイント、36パーセントポイント減少し、アポリポタンパク質B値はそれぞれ19パーセントポイント、15パーセントポイント、22パーセントポイント減少し、LDLコレステロール値はそれぞれ16パーセントポイント、14パーセントポイント、20パーセントポイント減少し、これらの結果は36週まで持続した。24週目には、ゾダシラン
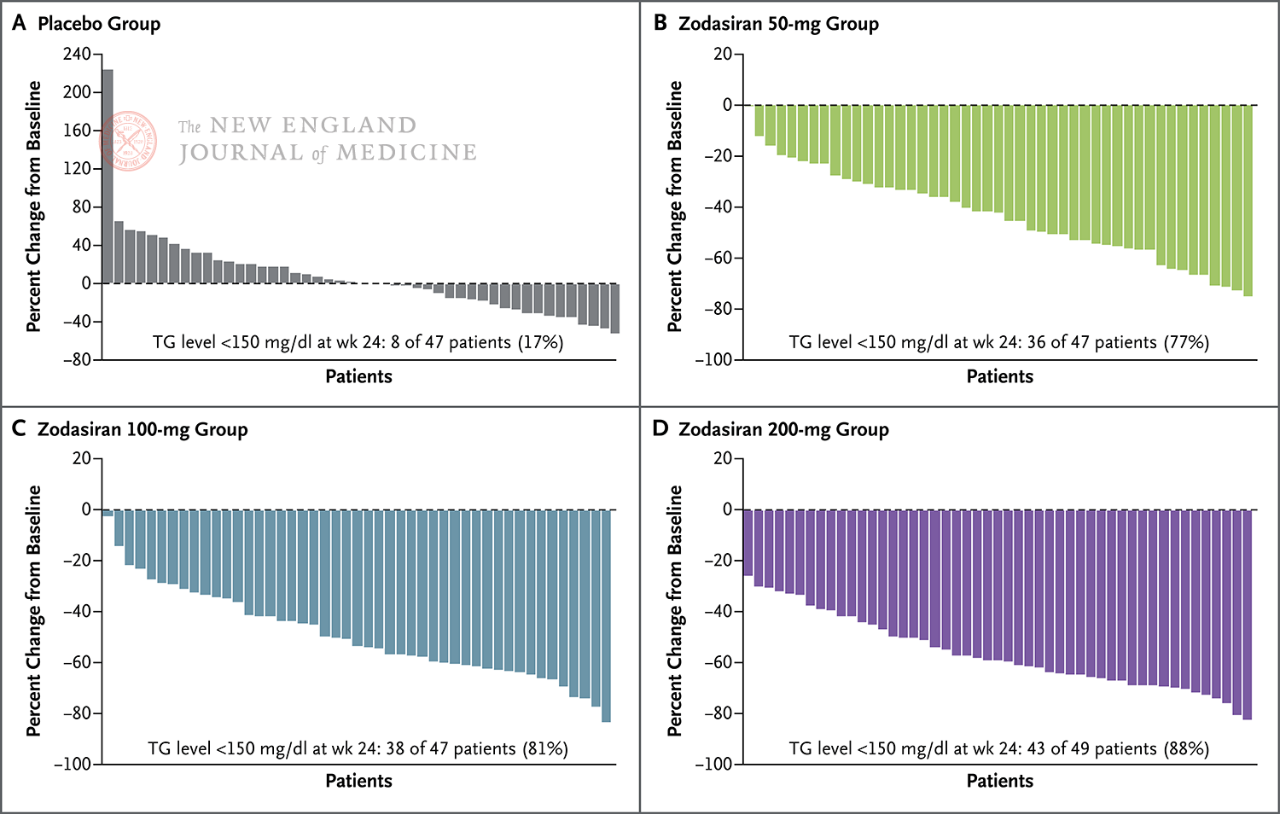
200 mg 群の患者の 88% において、空腹時 TG が正常範囲まで低下しました。
1日目と12日目の赤い矢印は、ゾダシランまたはプラセボの投与を示しています。
空腹時TG値は24週目に正常値まで低下した(150
mg/dL以下)
それぞれの柱は 1 人の患者を表します。
本試験では、ゾタシランは全用量群において安全であり、有害事象により試験を中止した患者は2名のみ(プラセボ群1名、ゾタシラン100mg群1名)であったことも確認された。ゾタシラン群における重篤な有害事象はすべて試験終了までに回復し、プラセボ群では1名が死亡した。懸念される唯一の有害事象は、プラセボと比較したゾタシラン200mg群におけるHBA1cの上昇であった(ベースラインから24週目までの平均変化率[±SD]:0.38±0.66% vs. 糖尿病既往患者における-0.03±0.88%)。糖尿病既往患者におけるHBA1cの上昇率は0.12±0.19% vs. -0.03±0.19%であった。
特に、本研究の対象患者のほぼ全員(96%)はスタチン(うち37%は高用量スタチン)による治療を受けており、1%はプロタンパク質変換酵素サブチリシン9阻害薬(PCSK9i)による治療を受け、21%はフィブラートによる治療を受けていました。したがって、ゾダシランを既存の治療レジメンに追加することで、依然としてかなりの脂質低下効果が得られ、これは将来、混合型高脂血症の治療における新たなレジメンとなる可能性があります。
本試験では、ゾタシランの最大用量である200mgを投与したところ、24週目にプラセボと比較して残留コレステロール値が34.4mg/dL低下しました。現在のモデルに基づくと、この低下により主要な心血管イベントが20%減少すると予測されます。ゾタシランは、患者の心血管イベントリスクを低減するために、全てのリポタンパク質成分に対する単剤療法として使用できる可能性があります。したがって、この薬剤が動脈硬化性疾患のリスクを低減する可能性を判断するには、さらなる研究が必要です。
NEJM誌に同時掲載された第2b相二重盲検ランダム化プラセボ対照MUIR試験では、別のsiRNA薬であるプロザシランを用いて混合型高脂血症を治療した[2]。プロザシランは、肝臓におけるアポリポタンパク質C3(APOC3)をコードする遺伝子の発現を低下させることで、TGおよび残留コレステロール値を低下させるように設計されている。本試験で観察されたTGおよび残留コレステロール値の減少は、ARCHES-2試験で認められたものと同様であった。したがって、混合型高脂血症患者において、両薬剤はトリグリセリドリッチリポタンパク質および残留コレステロール値を低下させる点で同様の効果を有すると推測される。
2 つの siRNA 研究の結果は、これが混合型高脂血症の治療に新たな選択肢をもたらし、患者の心血管疾患の転帰を改善する非常に有望なクラスの薬剤であることを示しています。
投稿日時: 2024年9月15日